2021-09-10
新陳代謝異常是癌症的一(yī)個主要标志(zhì)。異常的癌症代謝,如有氧糖酵解和增加的合成代謝途徑,在腫瘤的發生(shēng)、轉移、耐藥性和癌症幹細胞中(zhōng)起着重要作用。衆所周知(zhī)的緻癌信号通路, PI3K/AKT、Myc和Hippo通路,介導代謝基因的表達,增加代謝酶的活性。反之亦然,解除代謝途徑導緻細胞信号轉導途徑的缺陷,反過來爲抑制癌細胞增殖提供能量。正在進行的研究和臨床試驗集中(zhōng)于通過小(xiǎo)分(fēn)子或飲食幹預(如禁食、熱量限制和間歇性禁食)來抑制代謝酶。
腫瘤代謝表型特征
在20世紀20年代,Otto Warburg發現,與正常細胞不同的是,呼吸機制在癌細胞中(zhōng)受損,特别是在線粒體(tǐ)中(zhōng)。因此,癌細胞不使用氧化磷酸化(OXPHOS)。相反,它們通過糖酵解獲得ATP。即使在富氧的環境中(zhōng),它們也高度依賴于糖酵解(即有氧糖酵解)。
最近的研究顯示,癌細胞的線粒體(tǐ)可以保持完整,可以使用OXPHOS産生(shēng)能量。盡管有這種OXPHOS的能力,但許多類型的腫瘤仍依賴于有氧糖酵解來爲生(shēng)長和适應缺氧的腫瘤微環境。
腫瘤是由緻癌基因和腫瘤抑制基因的突變引起的。這些基因突變直接調控代謝酶的表達和活性。例如,c-MYC激活谷氨酰胺攝取,TP53調節癌細胞中(zhōng)的脂質代謝。癌細胞的異常代謝不僅僅是一(yī)種遺傳突變表型。它還直接影響腫瘤信号轉導途徑和細胞反應。基于這一(yī)概念,在許多研究和臨床試驗中(zhōng)研究針對特異性代謝表型的下(xià)一(yī)代抗癌藥物(wù)。
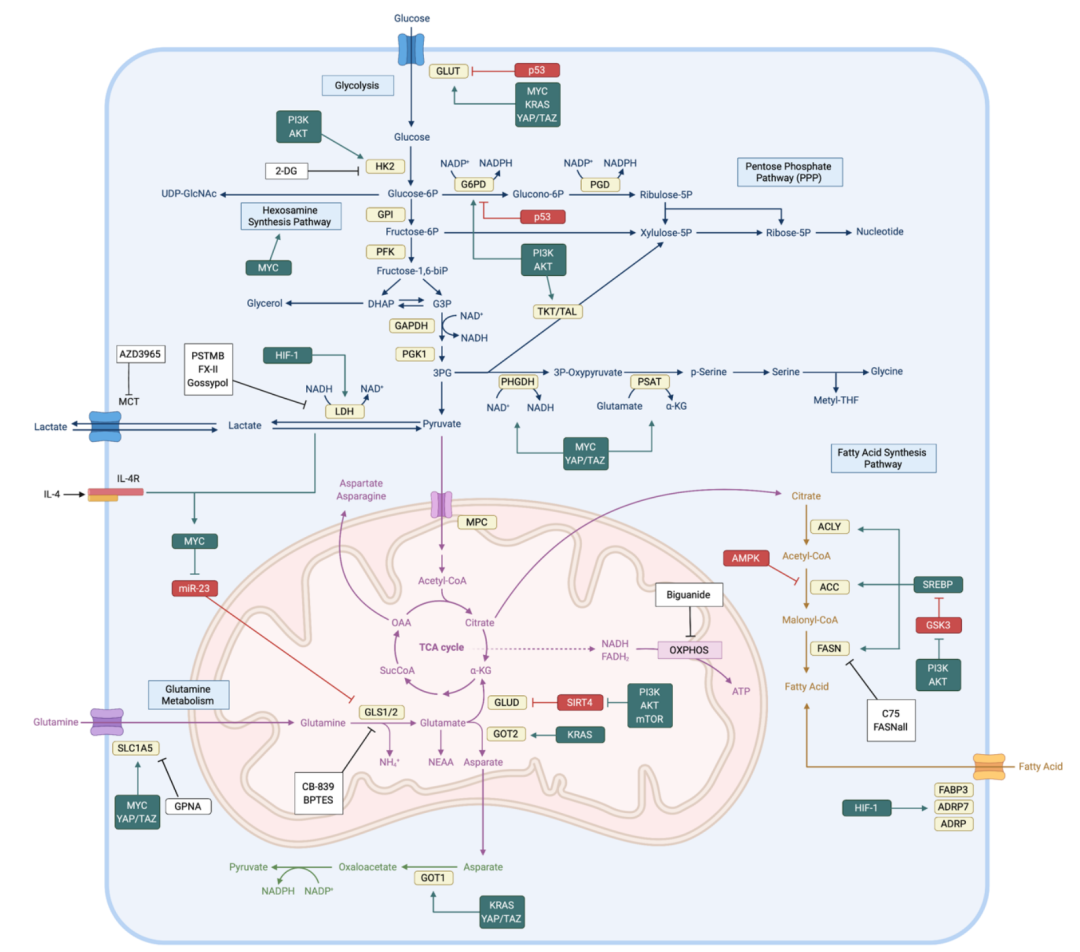
腫瘤代謝通路(Cells 2020, 9, 2308)
靶向代謝通路
葡萄糖、谷氨酰胺和脂肪酸代謝途徑中(zhōng)的代謝酶被認爲是有吸引力的藥物(wù)靶點。癌細胞上調糖酵解酶的表達及其酶活性,以促進有氧糖酵解。
2-Deoxy-Glucose (2DG)
2-脫氧葡萄糖(2DG),它結合并抑制HK2,降低糖酵解,并最終誘導多種癌症類型(如前列腺癌)中(zhōng)ROS介導的細胞凋亡。
抑制LDH
NAD+的再生(shēng)對于有氧糖酵解至關重要。LDH催化丙酮酸向乳酸轉化,再生(shēng)NAD+。抑制LDH酶活性的藥物(wù)正在被研究中(zhōng)。PSTMB通過抑制LDH誘導肺癌、乳腺癌、結腸癌和黑色素瘤細胞凋亡. FX-11, galloflavin, gossypol也通過LDH抑制,發揮抗癌作用。
乳酸
乳酸是有氧糖酵解的最終産物(wù),通過MCT-1轉運體(tǐ)分(fēn)泌到腫瘤微環境中(zhōng). 當與二甲雙胍聯合使用時,MCT-1抑制劑AZD3965可阻斷乳酸介導的腫瘤進展,并具有顯著的抗癌作用(NCT01791595)。
谷氨酰胺
谷氨酰胺代謝對不受抑制的癌症生(shēng)長也很重要。谷氨酰胺代謝參與多種細胞過程,包括三羧酸循環、脂肪酸合成和氧化還原穩态。阻斷營養物(wù)質的攝取是抑制特定代謝途徑的有力策略。GPNA和V-9302被開(kāi)發用于抑制谷氨酰胺轉運體(tǐ)SLC1A5,并在多種癌細胞系中(zhōng)具有抗癌作用。在線粒體(tǐ)中(zhōng),谷氨酰胺被GLS和其他轉氨酶轉化爲谷氨酸。CB-839(NCT03057600)在三陰性乳腺癌中(zhōng)抑制GLS并具有抗癌作用,此外(wài)非小(xiǎo)細胞肺癌(NCT04250545),複發性難治性多發性骨髓瘤的臨床也在招募中(zhōng)(NCT04250545,NCT03798678)。
脂肪酸
氨基乙酸(Aminooxyacetic acid,AOA)抑制轉氨酶活性,從而下(xià)調氨基酸和核苷酸的生(shēng)物(wù)合成. 從頭脂肪酸合成,對癌症進展的重要性。FASN介導脂肪酸合成的延伸步驟,是一(yī)個潛在的藥物(wù)靶點。FASN抑制劑FASNall可有效降低HER2+乳腺癌的腫瘤負擔。
甲戊酸途徑
膽固醇合成甲戊酸途徑在各種癌症類型中(zhōng)被高度解除調控。他汀類藥物(wù)最初被用作降膽固醇藥物(wù),通過下(xià)調甲戊酸途徑的限速酶HMG-輔酶a還原酶來抑制癌症生(shēng)長. 他汀類藥物(wù)的部分(fēn)抗癌作用是由于間接抑制了Hippo通路。甲戊酸途徑抑制可降低RhoAGTPase的脂化,從而抑制轉錄共激活因子YAP/TAZ。
氧化磷酸化
研究發現氧化磷酸化(OXPHOS)在癌細胞中(zhōng)是完好的,某些類型的癌症更依賴OXPHOS進行生(shēng)物(wù)能學。因此,線粒體(tǐ)OXPHOS抑制可能是藥物(wù)開(kāi)發的一(yī)個靶點。寡黴素和雙胍類藥物(wù)分(fēn)别通過抑制複合物(wù)V和複合物(wù)I來抑制線粒體(tǐ)電(diàn)子傳遞鏈,從而減少線粒體(tǐ)ATP的産生(shēng)。OXPHOS抑制劑對多種癌細胞都有抗癌作用。OXPHOS抑制介導的能量應激誘導了AMPK的激活。考慮到AMPK抑制細胞合成代謝,包括脂肪酸合成、甲戊酸途徑和GLUT1的表達,這些OXPHOS抑制劑可以同時抑制多種代謝途徑。
可塑性和聯合用藥
代謝可塑性可以通過上調其他代謝途徑來補償代謝限制,以避免應激反應。例如,二甲雙胍,一(yī)種2型糖尿病藥物(wù),通過抑制線粒體(tǐ)複合物(wù)I來抑制OXPHOS,但糖酵解作爲一(yī)種代償機制增加。研究結果表明,聯合治療可用來克服代謝可塑性。這些療法使用代謝途徑抑制劑的組合來防止代謝補償。谷氨酰胺在Myc誘導的肝癌中(zhōng)代謝上調。GLS抑制顯著增加了無腫瘤生(shēng)存率,但上調了轉酰胺酶、HK2、FASN和絲氨酸/甘氨酸合成等代償機制。聯合治療同時抑制這些通路可以協同抑制腫瘤生(shēng)長。
飲食調節與藥物(wù)幹預
癌細胞受到周圍環境的營養狀況的高度影響。由于食物(wù)攝取調節血液中(zhōng)的營養濃度,飲食組成是影響腫瘤微環境中(zhōng)代謝物(wù)濃度的主要因素。禁食協同增加了化療藥物(wù)的細胞毒性作用,。禁食模拟飲食(FMD)和間歇性禁食也會使抗癌藥物(wù)敏感,并具有顯著的抗癌作用。FMD通過幹擾氧化還原穩态促進癌症轉移,并激活腫瘤浸潤性淋巴細胞。同樣,間歇性禁食可抑制胰島素和IGF-1信号傳導。
與這些結果一(yī)緻的是,研究發現飲食幹預和代謝藥物(wù)之間存在協同效應。例如,二甲雙胍和間歇性禁食的聯合使用可有效地靶向癌症的代謝可塑性。該聯合治療通過MCL1-凋亡軸誘導細胞毒性作用。
小(xiǎo)編總結
腫瘤代謝異常是腫瘤的特征性标志(zhì),也是腫瘤耐藥的重要機制。闡明不同代謝背景下(xià)藥物(wù)療效的改變,不僅對未來的藥物(wù)開(kāi)發和臨床前研究很重要,而且對已經批準的藥物(wù)的重新臨床利用也很重要。新藥開(kāi)發加老藥的重利用,是靶向腫瘤代謝的主要藥物(wù)開(kāi)發策略。