2022-06-29
一(yī)、CAR-T細胞療法
CAR-T細胞療法是指嵌合抗原受體(tǐ)T細胞。CAR-T細胞免疫療法是新型治療腫瘤的精準靶向療法,也是未來攻克癌症腫瘤疾病的關鍵性技術之一(yī)。作爲腫瘤免疫治療的一(yī)種特異性療法,CAR-T是通過細胞基因工(gōng)程,利用識别腫瘤相關抗原抗體(tǐ)的嵌合蛋白(bái)與患者體(tǐ)内提取到的T細胞進行修飾,經過純化和大(dà)規模擴增之後的T細胞導入回患者體(tǐ)内後能特異性識别腫瘤細胞相關抗原靶點,激活人體(tǐ)免疫反應,殺滅腫瘤細胞。
利用基因工(gōng)程改造T細胞進而影響人體(tǐ)免疫反應的理念早在20世紀就被提出,但在2012年随着CAR-T療法在臨床實驗中(zhōng)成功治療了急性白(bái)血病。而迅速成爲全球研究熱點,并于2017年首次獲批上市。CARs根據胞内共刺激結構域的發展已經衍生(shēng)至5代,目前大(dà)多數公司的上市産品都屬于基于二代CAR-T技術進行探索開(kāi)發。
近年來CAR-T全球研究數量逐步增加,但大(dà)概有80%的CAR-T療法臨床試驗處于臨床前和臨床I期。CAR-T 細胞免疫療法的出現改變了血液腫瘤傳統以化療和放(fàng)療爲主的治療方式,目前大(dà)部分(fēn)該療法主要應用于血液腫瘤,而究其在治療血液惡性腫瘤中(zhōng)取得的顯著療效,和血液惡性腫瘤具有特異性靶點之間的密不可分(fēn)。其中(zhōng),最成功并且研究最多的是表達在大(dà)多數急性淋巴細胞白(bái)血病(ALL),慢(màn)性淋巴細胞白(bái)血病(CLL)和 B 細胞淋巴瘤中(zhōng)的 CD19 靶點,其他熱點靶點還有 CD20、CD30、BCMA、CD174 等。
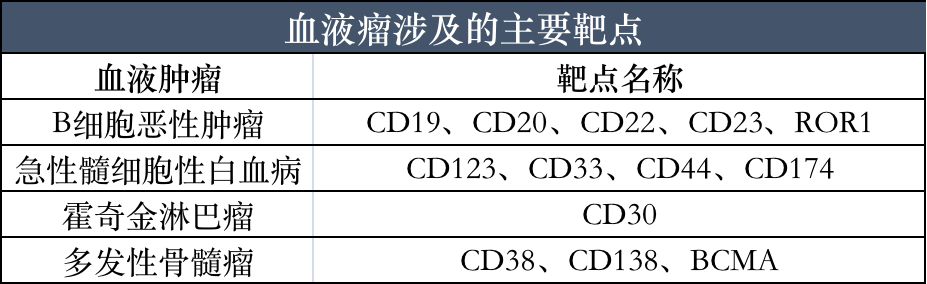
圖1:血液瘤涉及的主要靶點
截止到今日,全球範圍内共8款CAR-T産品上市。其中(zhōng)2款産品于國内上市。在歐美等國家已被廣泛應用于臨床。在美國,44% 的急性淋巴細胞白(bái)血病兒童患者接受 CAR-T 細胞治療的臨床應用,治愈率達到 60.6%;46% 的彌漫性大(dà) B 細胞淋巴瘤成人患者接受CAR-T 細胞治療,治愈率超過70%。
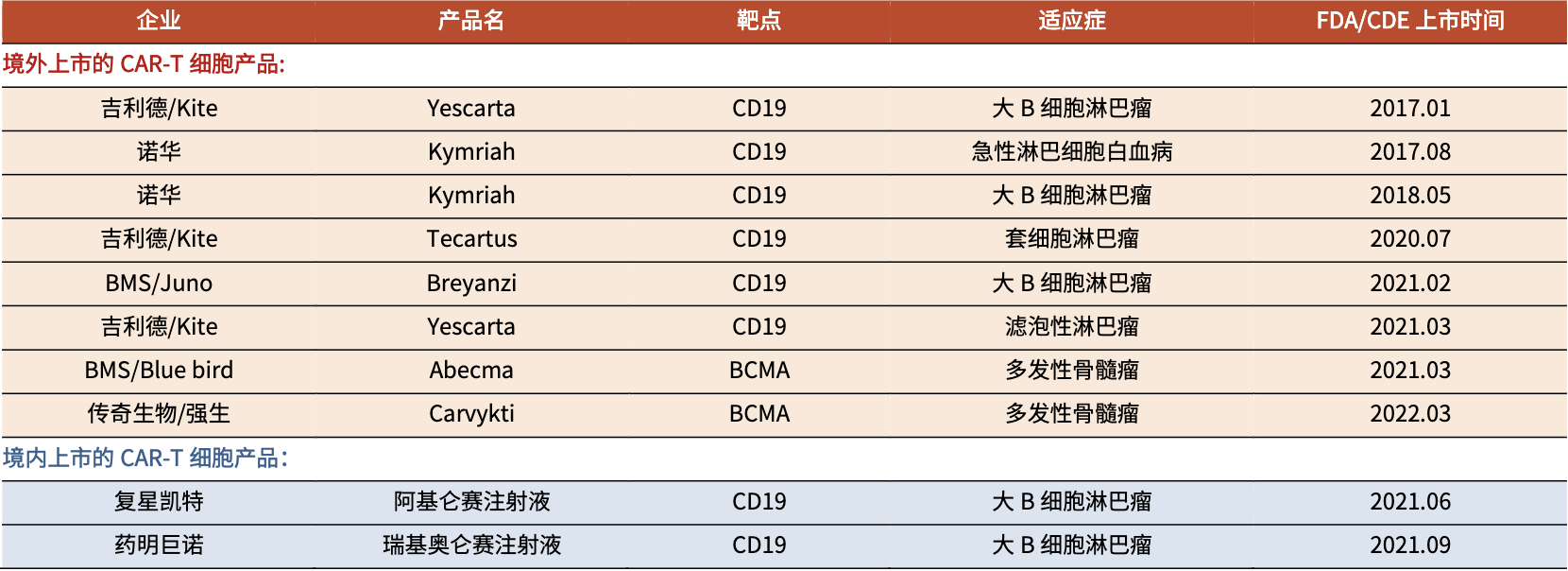
圖2:已上市的CAR-T細胞治療産品
二、CAR-T細胞療法的治療優勢
血液腫瘤是起源于造血系統的一(yī)大(dà)類惡性腫瘤,主要包括多發性骨髓瘤、白(bái)血病和淋巴瘤,其中(zhōng)淋巴瘤可分(fēn)爲非霍奇淋巴瘤和霍奇淋巴瘤。血液瘤中(zhōng)以非霍奇淋巴瘤發病率最高,彌漫性大(dà)B細胞淋巴瘤是非霍奇淋巴瘤最常見的一(yī)種病症。IARC發布的數據顯示,2020年世界血液瘤新發病例約128萬,死亡病例數達到65萬。同時血液腫瘤一(yī)線治療後複發率較高,以彌漫性大(dà)B細胞淋巴瘤爲例,30%-40%的患者會出現耐藥或疾病複發情況。
在CAR-T細胞治療出現之前,血液腫瘤的治療方式多以放(fàng)化療爲主,對比傳統療法,選擇CAR-T療法治療血液腫瘤,無論是從治療潛力還是治療效果來說,都爲更佳選擇。
3、優異的治療效果。CAR-T 細胞療法已顯示出比其他治療方案更适合靶向特定疾病或按所需功能定制的潛力。CAR-T 細胞通過其 CAR 結構,能夠特異性靶向多個腫瘤相關靶點,進而更精确地靶向不同腫瘤細胞。
三、CAR-T細胞療法的局限性
目前CAR-T細胞療法目前主要應用在末線血液惡性腫瘤治療中(zhōng),對于傳統治療手段已經失效的末線患者來說彌補了治療空缺。與傳統血液瘤治療相比,CAR-T療法因具有隻需一(yī)次注射,一(yī)次用藥,治療周期短,對患者的創傷小(xiǎo),副作用小(xiǎo),治療周期短,治療精準度高等特點備受矚目,但同時CAR-T細胞療法也面臨着諸多問題與挑戰。
首先是市場化方面,一(yī)個“貴”字足以涵蓋CAR-T細胞療法目前的困局。首先這個“貴”是指價格,目前全球共有8款CAR-T細胞治療産品上市,其中(zhōng)在國内上市的兩款CAR-T産品阿基侖賽注射液和瑞基奧侖賽注射液,分(fēn)别定價爲120萬元(人民币)和129萬(人民币),相對于國外(wài)上市的産品,已經算得上是“良心價格”。但抛去(qù)其他可能會産生(shēng)的影響來說,以這個價格來說,對于大(dà)部分(fēn)家庭,已經是相當昂貴的費(fèi)用,而且這僅爲藥品價格,CAR-T細胞治療整體(tǐ)費(fèi)用包括藥品費(fèi)用、治療護理費(fèi)用、重症監護室費(fèi)用以及其他費(fèi)用,其中(zhōng)治療護理費(fèi)用也包括預防/治療在整個療程中(zhōng)出現的副作用及配套治療方案,比如常見副作用(細胞因子風暴CRS和毒副作用ICANS),非藥品和藥品的費(fèi)用基本相當,這也導緻CAR-T細胞治療産品不太能走進“尋常百姓家”。
其次,凡事都要講究一(yī)個“兵貴神速”,目前已上市CAR-T細胞療法均源于自體(tǐ),使用患者自身特定的 T 細胞需要時間,目前已上市産品進行制造生(shēng)産周期在半個月到一(yī)個月之間。此外(wài)患者由于身體(tǐ)健康狀況,可能無法提供足夠的T細胞。因爲病人在接受CAR-T治療之前,大(dà)部分(fēn)都會接受過化療等細胞毒性治療,導緻T細胞數量下(xià)降,進一(yī)步增加了周期長度。長期的制備時間,也是CAR-T細胞治療産品的局限之一(yī)。
除了以上兩種局限,CAR-T細胞療法作爲新型療法,影響其發展的因素還有很多,安全性、癌種局限性、相關政策的成熟度、規模化等痛點也是十分(fēn)清晰。
2、癌種局限性。盡管 CAR-T 療法在治療血液惡性腫瘤上取得了可喜進展,但其在治療實體(tǐ)瘤過程中(zhōng)仍面臨諸多巨大(dà)挑戰,CAR-T 細胞治療實體(tǐ)瘤的療效目前不如在血液腫瘤中(zhōng)效果顯著。主要原因有兩點:第一(yī),實體(tǐ)瘤異質性高,缺乏适合CAR-T治療的細胞表面靶點;第二,實體(tǐ)瘤具有強烈抑制免疫的微環境。
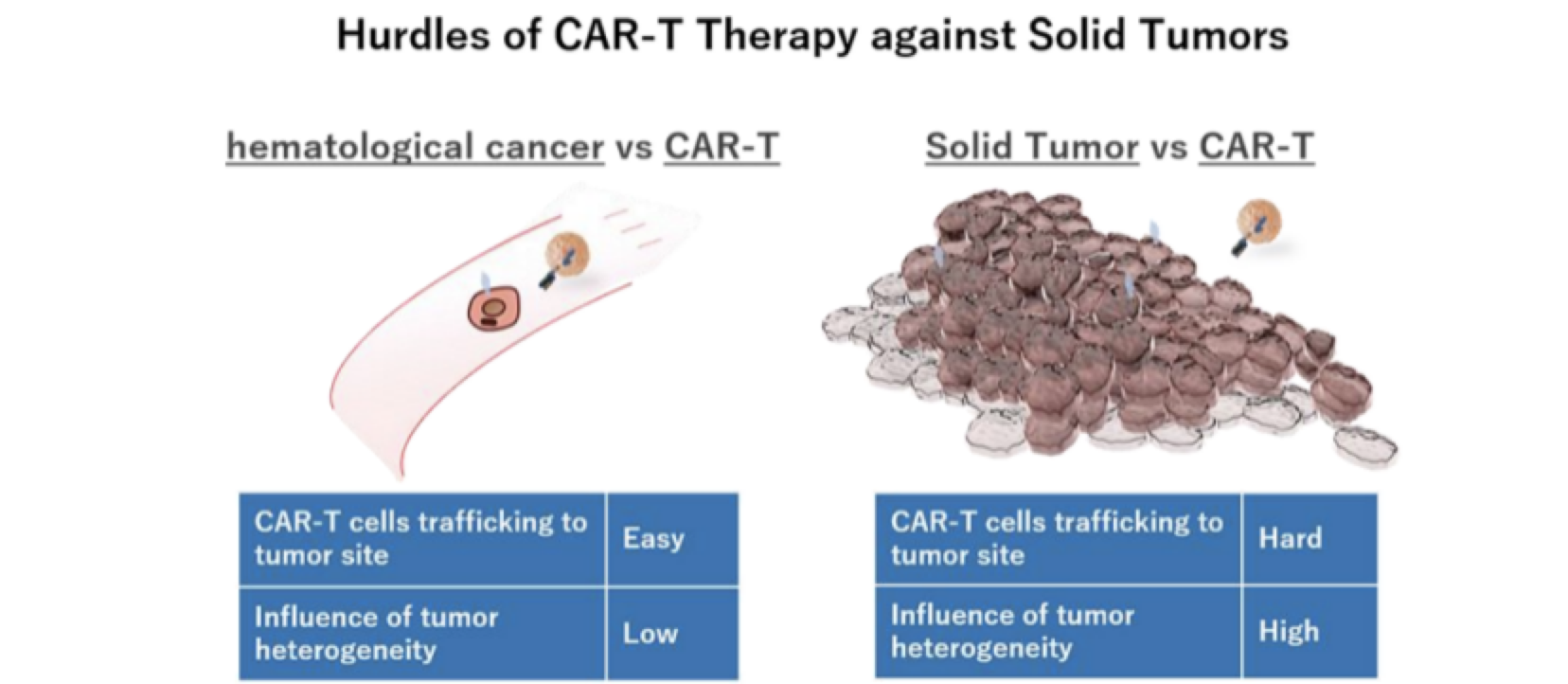
圖3:CAR-T藥物(wù)實體(tǐ)瘤治療局限性
在監管方面,中(zhōng)國對于CAR-T療法是屬于藥品還是醫療技術,監管權屬于國家藥監局還是國家衛健委研讨多年,2020年國家藥品監督管理局CDE發布《人源性幹細胞及其衍生(shēng)細胞治療産品臨床試驗技術指導原則(征求意見稿)》,明确了将幹細胞療法按照藥物(wù)管理,爲CAR-T療法的監管進一(yī)步明确方向。但相對來說,由于CAR-T細胞療法屬于新興技術,在生(shēng)産與監管方面依舊(jiù)存在諸多問題,值得探讨與改進。
4、規模化。目前,不同公司的自體(tǐ)CAR-T細胞産品在生(shēng)産制備中(zhōng)使用的方法各異,但基本的生(shēng)産流程大(dà)體(tǐ)類似,主要包括T細胞篩選與富集、T細胞活化、T細胞基因轉導、T細胞擴增以及T細胞冷凍保存等5大(dà)步驟。CAR-T細胞的生(shēng)産流程環環相扣,任何一(yī)環的疏忽都會對最終産品的安全性、純度以及效力産生(shēng)深遠影響。目前,CAR-T産品的每個生(shēng)産環節都具有許多技術方法可供選擇,難以建立标準化的工(gōng)藝參數及條件,因此如何制定具有自動化、規模化且一(yī)緻化的生(shēng)産方案任重道遠。
四、CAR-T細胞療法如何破局
自CAR-T療法上市以來,産品銷售額持續增長,以2017年上市的兩款産品爲例,2017-2020年諾華公司的Kymriah全球銷售額年複合增長率達329%,凱特公司的Yescarta全球銷售額的年複合增長率達到331%。全球CAR-T細胞治療市場從2017年的0.1億美元增長到2021年的18億美元。但對于CAR-T細胞治療産品的投入來說,依舊(jiù)是“入不敷出”。
作爲潛力熱門賽道,越來越多的企業加入了競争。但如何直擊痛點,成功破局,成爲了大(dà)家讨論的熱點。
首先依舊(jiù)是咱們之前讨論過的“貴”,CAR-T細胞治療産品的價格上的貴,主要受兩方面影響:一(yī)是目前已上市的産品數量少,缺少競争,其他治療血液瘤的産品的效果不及CAR-T細胞治療産品,在競争少、效果好的強效光環加持下(xià),會造成産品價格偏高,無法用于更多患者的治療中(zhōng);二是CAR-T細胞治療産品屬于新型療法,從采集患者的免疫細胞、體(tǐ)外(wài)細胞培養、轉染、擴增和回輸等制備和治療。由于試劑等耗材成本、CAR-T細胞的質控檢測成本、細胞産品GMP廠房運營成本、第三方認證和質檢的費(fèi)用都很高,目前終端成本很難下(xià)降,而且CAR-T産品并沒有進入醫保,相關的商(shāng)業保險項目也是少之又(yòu)少,這也導緻了其價格居高不下(xià)。
不過,目前國内有越來越多的企業進入到了CAR-T産品的研發之中(zhōng),如複星凱特、藥明巨諾、傳奇生(shēng)物(wù)、永泰生(shēng)物(wù)、科濟生(shēng)物(wù)、上海細胞集團等,相關臨床試驗也呈井噴之勢。
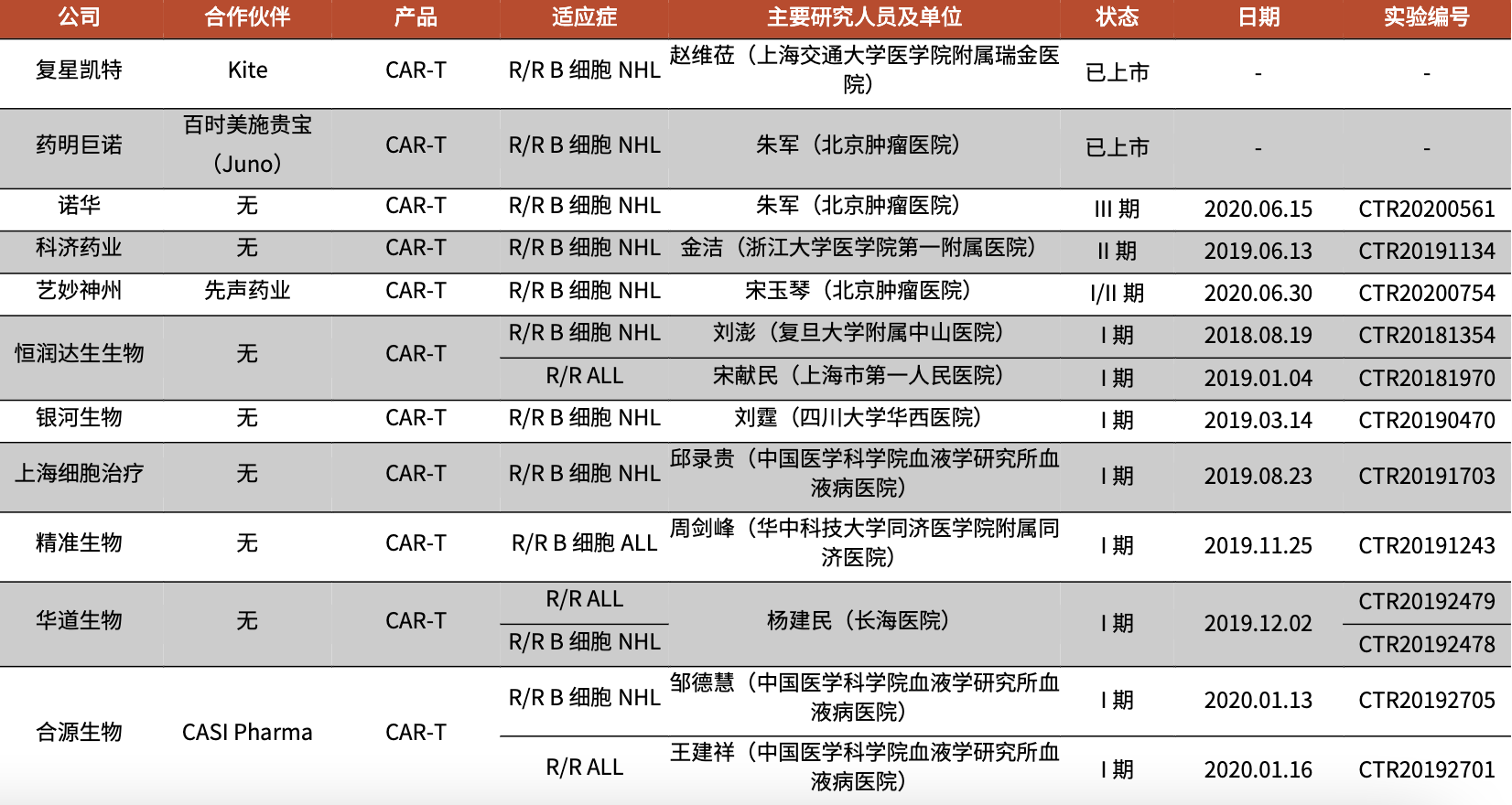
圖4:國内靶向CD19的CAR-T産品管線
就像是PD-1一(yī)樣,之前也有着“神藥天價”之名,随着越來越多的産品成功上市,且有4款國産PD-1藥物(wù)陸續進入醫保目錄,曾經的“天價藥”逐漸爲更多患者帶來“福音”。而且在19年,美國國家醫保機構Medicare于就确定了CAR-T産品的門診報銷方案,特定患者自費(fèi)比例降低80%,成爲CAR-T推廣的重大(dà)利好。如果CAR-T也能有更多的産品進入市場,且能成功進入醫保,将惠及到更多的腫瘤患者,這也将更好地推動CAR-T産品的市場發展。
而根據弗若斯特沙利文預測,2021年中(zhōng)國CAR-T市場規模約爲2億元,到2024年将增長至53億元,至2030年市場規模有望達到289億元,中(zhōng)國有望在未來短時間内彎道超車(chē),占據大(dà)一(yī)部分(fēn)全球市場份額。
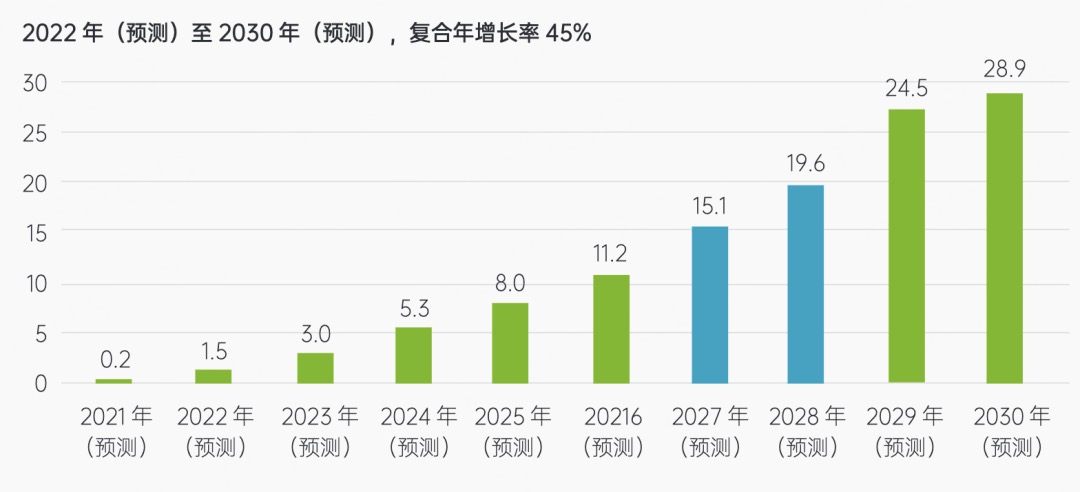
圖5:CAR-T細胞療法中(zhōng)國市場規模預測(十億元)
除了價格上的“貴”,速度上的“貴”也未來可期。
從 2002 年起,許多科學家緻力于修飾、改造 CAR-T 結構的胞内信号轉導區,以進一(yī)步提高治療效果。根據“共刺激分(fēn)子序列”結構的不同,CAR-T 細胞分(fēn)爲五代,目前已上市産品均爲第二代,特點是添加了共刺激結構域 CD28或 4-1BB。
而第三代含有兩個共刺激結構域、三個胞内信号組分(fēn)(CD3ζ、CD28、4-1BB或 OX40)。三代 CAR 結構使細胞具有更強的腫瘤抑制、裂解能力。第四代添加了自殺基因,可在具有免疫抑制性的腫瘤微環境中(zhōng)釋放(fàng)促炎性因子,從而招募并活化更多的免疫細胞、增強免疫反應。
當然最終目的還是第五代——通用型 CAR-T 細胞,突破個體(tǐ)限制,實現規模化生(shēng)産和治療。包括:通用 CAR 設計和通用 T 細胞設計。
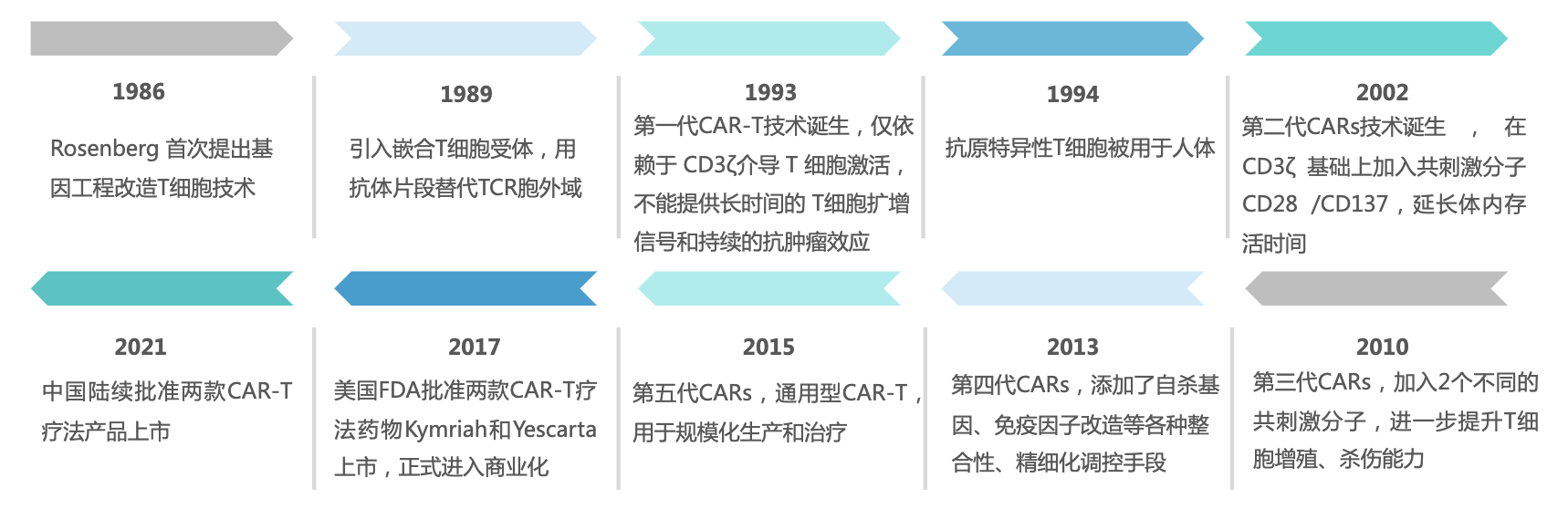
圖6:CAR-T技術發展曆程
目前處于研究中(zhōng)的解決方案是通過生(shēng)産 “通用型”CAR-T 産品降低成本,異體(tǐ)的問題是會産生(shēng)免疫排斥以及宿主移植病,解決方案是通過 CRISPR Cas9 等基因編輯工(gōng)具敲除或者破壞 HLA 和 TCR 相關功能基因。生(shēng)産周期方面,曆經從病人取樣、運輸、生(shēng)産及擴增、質量檢測及放(fàng)行,時間一(yī)般長達 3 周以上。從産品特性來看,通用型CAR-T療法不受限于細胞來源,并且具備規模化效應,理論上能夠解決大(dà)部分(fēn)障礙。
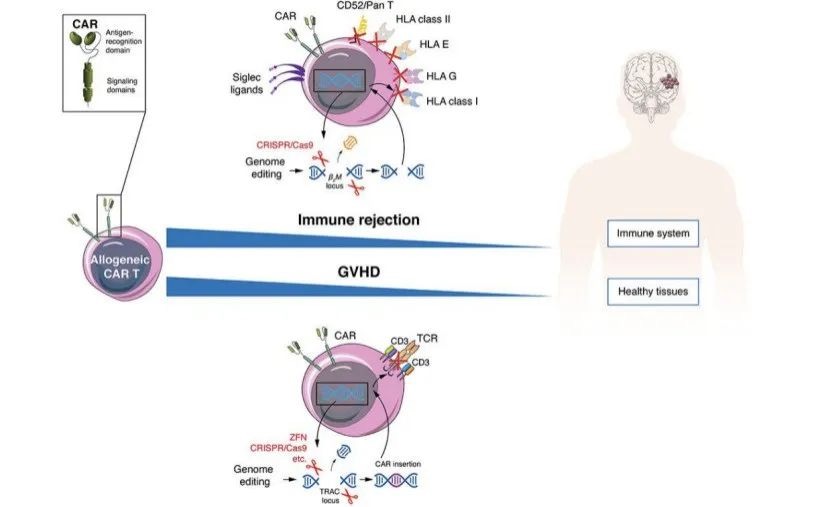
圖7:“通用型”CAR-T問題及解決方案
對于一(yī)些晚期嚴重疾病患者而言,延遲治療通常也會造成一(yī)定的問題。目前的階段方案均處于臨床階段,比如諾華的 TCharge 平台和亘喜生(shēng)物(wù)的 FasTCAR 平台通過簡化激活和轉導步驟,并把主要增殖階段轉移到人體(tǐ)内,實現僅需兩天左右的制備期。制備時間大(dà)大(dà)縮短,也可以更及時地應用到治療之中(zhōng)。
除了以上兩個方面的“破局之法”,在其他方面,CAR-T細胞治療産品也有着許多需要改進的地方,例如:副作用怎麽降低、适應症的拓展等。目前也取得了部分(fēn)成果。
1、降低副作用
CAR-T 細胞療法的相關安全性問題主要是脫靶毒性和細胞因子風暴。目前遇到此問題主要解決方案爲:輕度 CRS 通過退熱治療及時評估以排除其他病因,并進行抗生(shēng)素治療以避免感染;重度 CRS 采用皮質類固醇、托珠單抗及抗 IL-1 治療(如阿那白(bái)滞素);神經系統事件用抗癫痫藥物(wù)處理;感染并發症用抗菌藥物(wù)治療,防止中(zhōng)性粒細胞減少。
除了目前的解決方法,尋找更爲嚴格的腫瘤特異性抗原作爲靶點,顯然是更好的處理方式,目前諾華申請多個和CAR-T細胞治療的脫靶問題處理、減少細胞因子風暴等相關專利。
2、實體(tǐ)瘤研發進展
由于 CAR-T 在治療血液腫瘤方面表現突出,被普遍認爲是人類最有希望最終攻克癌症的創新療法之一(yī)。盡管目前沒有針對實體(tǐ)瘤的 CAR-T 産品上市,在臨床研究階段部分(fēn)産品有了不錯的進展,在攻堅實體(tǐ)瘤方面,各國生(shēng)物(wù)技術公司都在不斷努力。
①胃癌、胰腺癌等。2022年5月9日,科濟藥業針對 Claudin18.2的CAR-T細胞産品CT041,治療消化系統腫瘤的研究結果發表在國際頂級期刊《Nature Medicine》雜(zá)志(zhì)上,這也算是首個發表于頂級學術期刊的迄今爲止最大(dà)樣本量的CAR-T細胞治療實體(tǐ)瘤的臨床研究。在療效方面,36例具有腫瘤靶病竈的患者中(zhōng),31例患者觀察到不同程度的目标病竈縮小(xiǎo),總客觀緩解率(ORR)爲48.6%,疾病控制率(DCR)爲73.0%。所有胃癌患者總客觀緩解率爲57.1%,疾病控制率達75.0%,這個成績可謂是相當亮眼。此外(wài),CLDN 18.2活化還可見于食管癌、卵巢癌和肺腺癌中(zhōng),因此是具有潛力治療癌症的熱門靶點。

圖8:CT041研究結果在《Nature Medicine》發表
②肺癌。目前已進入肺癌治療臨床試驗的CAR-T療法的靶抗原包括CEA、DLL3、EGFR、GPC3、HER2、MSLN、MUC1、PD-L1、PSMA和ROR1等,大(dà)多尚處于臨床I期研究階段。除此之外(wài),靶向CD47、EphA2、LunX和MAGE-A1的CAR-T也在臨床前研究中(zhōng)展現了對肺癌細胞的強大(dà)殺傷能力。
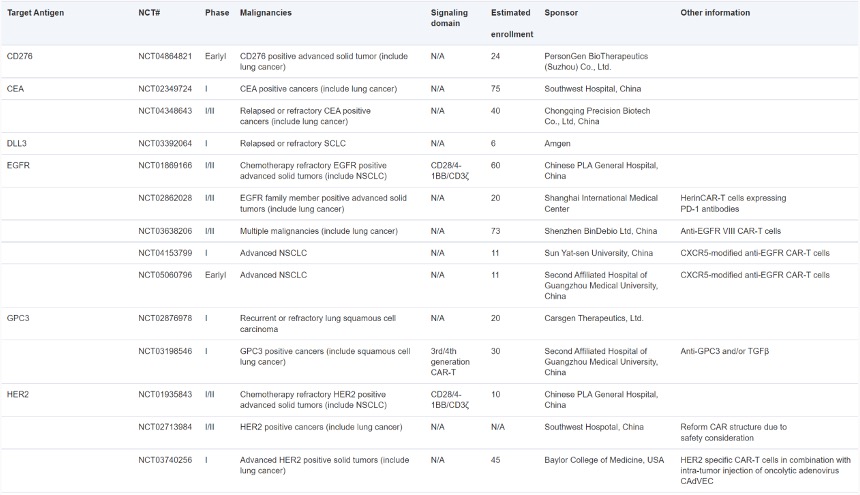
圖9:CAR-T細胞治療肺癌的臨床試驗
③肝癌。HCC中(zhōng)的CAR-T療法靶點有GPC3、AFP、c-Met、MUC1、EpCAM、CD133、CD147、NKG2D、CEA等。
上海交通大(dà)學醫學院附屬仁濟醫院所開(kāi)展的兩項連續的I期研究對GPC3 CAR-T療法在HCC中(zhōng)的應用進行了探索,研究共納入13例晚期HCC患者,3年、1年和6個月總生(shēng)存(OS)率分(fēn)别爲10.5%、42.0%和50.3%,其中(zhōng)1例患者在44.2個月後仍存活。9例患者發生(shēng)細胞因子釋放(fàng)綜合征(CRS),其中(zhōng)8例爲1-2級,1例爲5級,未發生(shēng)3級或4級神經毒性。其他數項評估GPC3 CAR-T單獨治療或聯合免疫檢查點抑制劑或聯合抗血管生(shēng)成藥物(wù)在HCC中(zhōng)療效與安全性的研究正在進行中(zhōng)。
之前有研究團隊構建了CD133特異性CAR-T細胞(CART-133),并發現CART-133細胞具有較強的細胞裂解能力,并可顯著抑制體(tǐ)内腫瘤生(shēng)長。随後,該團隊進行了一(yī)項開(kāi)放(fàng)标簽單臂I/II期臨床試驗,以評估CART-133細胞對晚期HCC等癌症患者的抗腫瘤作用。該研究I期納入23例患者,包括14例HCC患者,其中(zhōng)9例患者病情穩定,6個月疾病控制率爲43%[6]。該研究的II期階段共納入21例HCC患者,患者中(zhōng)位OS爲12個月(95%CI,9.3-15.3個月),中(zhōng)位無進展生(shēng)存期(PFS)爲6.8個月(95%CI,4.3-8.4個月)。1例患者達到部分(fēn)緩解(CR),14例達到疾病穩定(SD)。患者發生(shēng)3級貧血2例,3級高膽紅素血症4例,未見4級AE[7]。
此外(wài),其他靶點均有相關臨床研究正在進行中(zhōng)。
④結直腸癌。2022年4月19日,斯丹賽生(shēng)物(wù)宣布,FDA已授予GCC19CART快速通道資(zī)格。斯丹賽介紹的2個劑量爬坡試驗組21例患者的數據,驗證了GCC19CART産品的安全性和初步療效。其中(zhōng)13患者以1級劑量(1x106 cells/kg)入組,8名患者以2級劑量(2x106 cells/kg)入組。根據實體(tǐ)腫瘤療效評價标準(RECIST1.1),1級劑量組客觀緩解率(ORR)爲15.4%(2/13),2級劑量組客觀緩解率爲50%(4/8)。受試患者最常見的不良反應事件是細胞因子釋放(fàng)綜合征(CRS)和腹瀉,2例患者出現神經中(zhōng)毒,經皮質類固醇治療後得到緩解。總的來說,GCC19CART在複發/難治性結直腸癌患者中(zhōng)顯示出與劑量相關的良好的臨床初步療效以及可接受的安全性。
⑤腦瘤。近期,CAR-T細胞療法的臨床試驗結果再次登上國際頂級期刊《Nature》雜(zá)志(zhì)。針對緻命的實體(tǐ)腦瘤,CAR-T細胞療法再次帶來治療曙光:接受治療的患者,75%可以從治療中(zhōng)獲益,癌症症狀得到緩解。研究人員(yuán)表示,如果将靜脈注射改爲腦室内注射,有望進一(yī)步降低患者全身性的副作用發生(shēng)率,比如降低CAR-T細胞治療最常見的副作用細胞因子風暴的發生(shēng)率等。

圖10:《Nature》雜(zá)志(zhì)刊登CAR-T細胞療法治療腦瘤臨床試驗
⑥卵巢癌。2021年,中(zhōng)國的創新性的CAR-T細胞療法治療實體(tǐ)瘤的治療成果登上了國際一(yī)流學術期刊《Journal for ImmunoTherapy of Cancer》(《癌症免疫治療雜(zá)志(zhì)》)。在這項研究中(zhōng),上海細胞治療團隊打造的白(bái)澤T細胞治療技術,通過讓CAR-T細胞自分(fēn)泌PD-1抗體(tǐ),成功幫助一(yī)名晚期卵巢漿液性腺癌女性患者延長了生(shēng)存期,患者總生(shēng)存時間達到17個月。在此次治療中(zhōng)患者并未出現諸如發熱、寒戰、嘔吐和肌肉酸疼等副作用,僅出現了高血壓1級和乏力等輕微副作用。
除了以上幾種實體(tǐ)瘤,黑色素瘤、膠質母細胞瘤、乳腺癌、胰腺癌等不同部位的實體(tǐ)瘤也有不同程度的進展。相信随着研究的不斷進展,CAR-T 細胞療法會在實體(tǐ)瘤治療領域有更多新的突破。
CAR-T細胞療法作爲“後起之秀”,已經有源源不斷的企業正在投身其中(zhōng),随着全球CAR-T技術研發的不斷深入、支付體(tǐ)系逐步完善、以及通用型細胞療法的不斷發展,未來CAR-T的臨床适應症将不斷擴充,作爲未來的發展方向之一(yī),希望CAR-T細胞療法可以通過正在進行的研究,降低毒副作用,降低醫療成本,增加有效性和範圍,提高安全性并有效生(shēng)産,突破實體(tǐ)瘤的瓶頸,讓越來越多的晚期癌症患者可以從中(zhōng)獲益,給更多的人帶來“生(shēng)”的希望。

想了解更多,請關注誇克醫藥微信公衆号